Главное меню
Вы здесь
Виды и особенности коррозионных разрушений сварных соединений
Виды и особенности коррозионных разрушений сварных соединений
Виды и особенности коррозионных разрушений металлических, в том числе сварных, конструкций определяются свойствами материала, напряженным состоянием в конструкции, свойствами коррозионной среды и условиями взаимодействия металла со средой (температурой, временем, условиями контактирования, давлением и др.). Механизм коррозионных разрушений сварных соединений не отличается от механизма разрушений основного металла. Особенности, которые определяют (в отличие от основного металла) причины, характер, кинетику и механизм разрушений сварных соединений, зависят от физико-химического воздействия сварки, вызывающего неблагоприятное изменение и неоднородность свойств металла и напряженного состояния, следствием чего является усиление отрицательного воздействия среды.
Для сварного соединения характерны:
- а) структурно-химическая макро- и микронеоднородность (основной металл, литой металл шва, переходные структурные зоны влияния; зерна, границы зерен, фазы включения и т. д. в пределах каждой зоны);
- б) неоднородность напряженного состояния собственного (остаточные напряжения и пластическая деформация) и от внешней нагрузки;
- в) геометрическая неоднородность (технологические и конструктивные концентраторы).
Эти основные виды неоднородности определяют механическую, физическую и электрохимическую макро- и микронеоднородность сварных соединений (рис. 1) и особенности коррозионных разрушений сварных соединений (рис. 2).
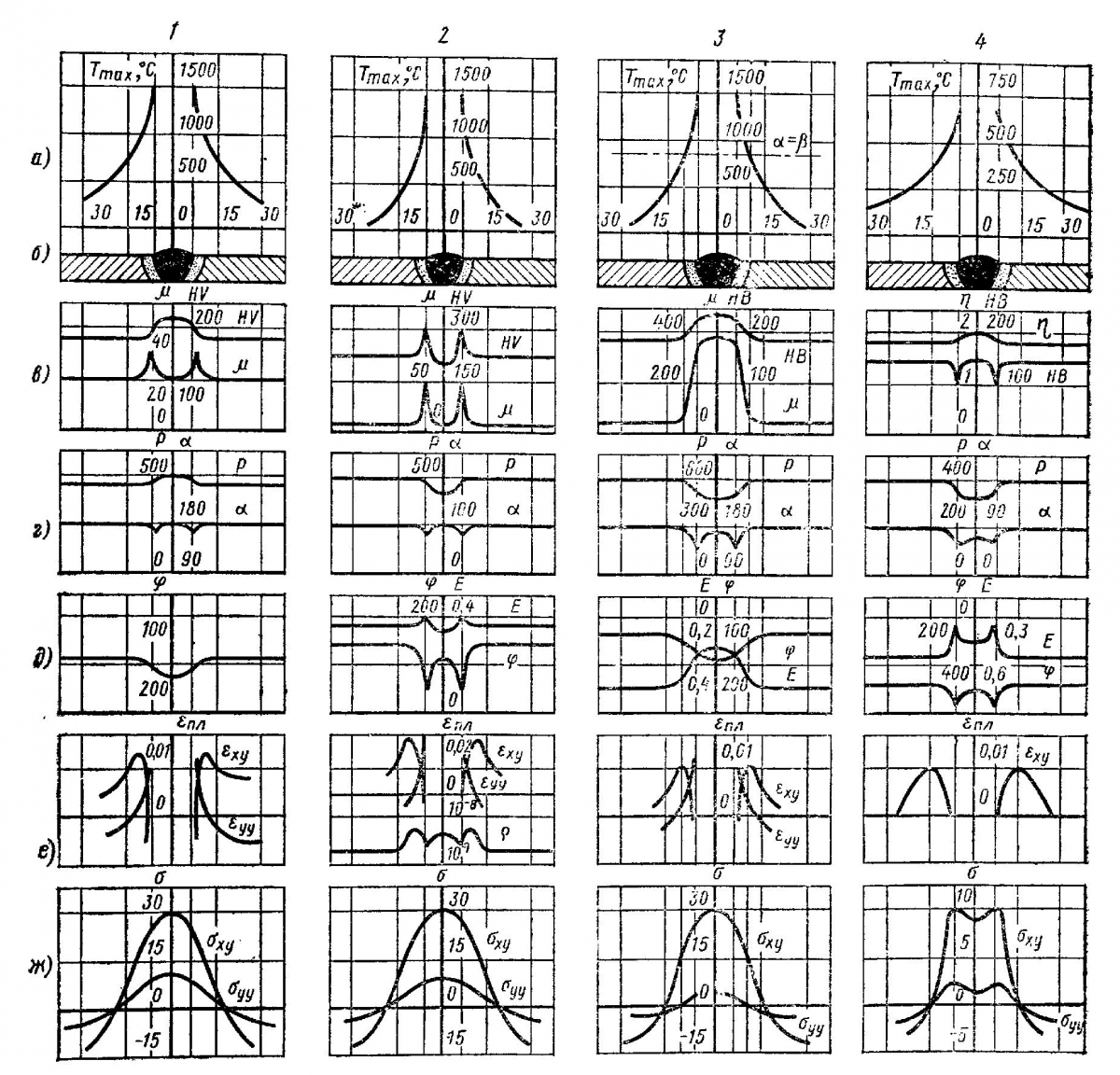
Рис. 1. Неоднородность сварных соединений в поперечном сечении: а – максимальные температуры; б – схемы сварного соединения; в – твердости HV, HB, величина μ зерна и плотность η окисной пленки; г – механические свойства при изгибе; Р – несущая нагрузка, кгс; α – угол изгиба; д – электродный φ и термоэлектрический Е потенциалы, мВ; е – остаточные пластические продольные εxy и поперечные εyy деформации; ρ – ориентировочная плотность дислокаций; ж – остаточные продольные σxy и поперечные σyy напряжения, кгс/мм2:
1 – СтЗсп; 2 – 12Х18Н10Т; 3 – ВТ1-1; 4 – АМг6, δ = 3 мм, аргонодуговая сварка вольфрамовым электродом
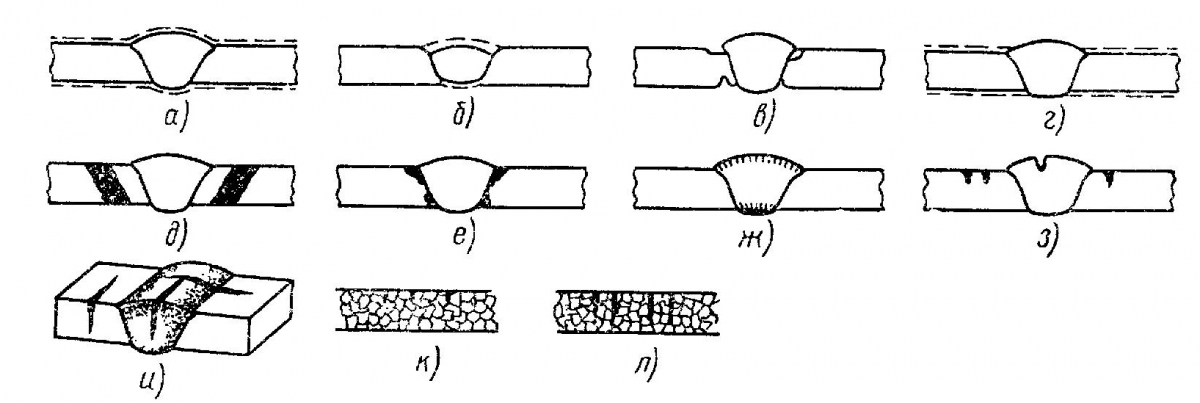
Рис. 2. Виды разрушений сварных соединений: а – г – соответственно общая коррозия: равномерная, сосредоточенная на шве, сосредоточенная в зоне термического влияния, преимущественно основного металла; д – з – соответственно местная коррозия: межкристаллитная в зоне термического влияния, ножевая в зоне сплавления, в сварном шве и точечная; и – л – коррозионное растрескивание и усталость меж- н транскристаллитные
По механизму различают коррозию химическую и электрохимическую. Химическая коррозия представляет собой процесс взаимодействия металла с агрессивным компонентом среды (сухими газами, неэлектролитами) по реакции Ме+x→Ме x. Электрохимическая коррозия – процесс самопроизвольного разрушения металла в результате электрохимических реакций, скорость которых определяет скорость коррозии:
- а) анодной реакции – перехода ионов металла Ме+ в раствор с оставлением эквивалентного количества n электронов е в металле; Ме0–nе→Меn+, определяющей материальные потери при коррозии;
- б) катодной реакции – процесса восстановления окислительных компонентов среды D (Н+, О2, Сl2, Br2, NО-3 и др.) за счет присоединения появившихся в металле избыточных электронов (процесс деполяризации D+ ne→ (Dne);
- в) процесса перетекания электронов по металлу и соответствующего перемещения катионов (+) и анионов ( – ) в растворе, т. е. коррозионного тока.
В подавляющем большинстве сред процесс коррозии является электрохимическим.
По виду коррозионных разрушений различают
- общую (сплошную) коррозию (равномерную, неравномерную, избирательную);
- местную (локализованную в виде язв, точек, под поверхностью, межкристаллитную);
- растрескивание под действием статических и циклических нагрузок.
Особенности общей электрохимической коррозии сварных соединений связаны с электрохимической неоднородностью двух видов:
- а) макронеоднородностью, обусловленной различием химического состава и структуры в разных зонах соединения;
- б) микронеоднородностью, обусловленной структурной и химической неоднородностью в пределах каждой зоны (рис. 3).
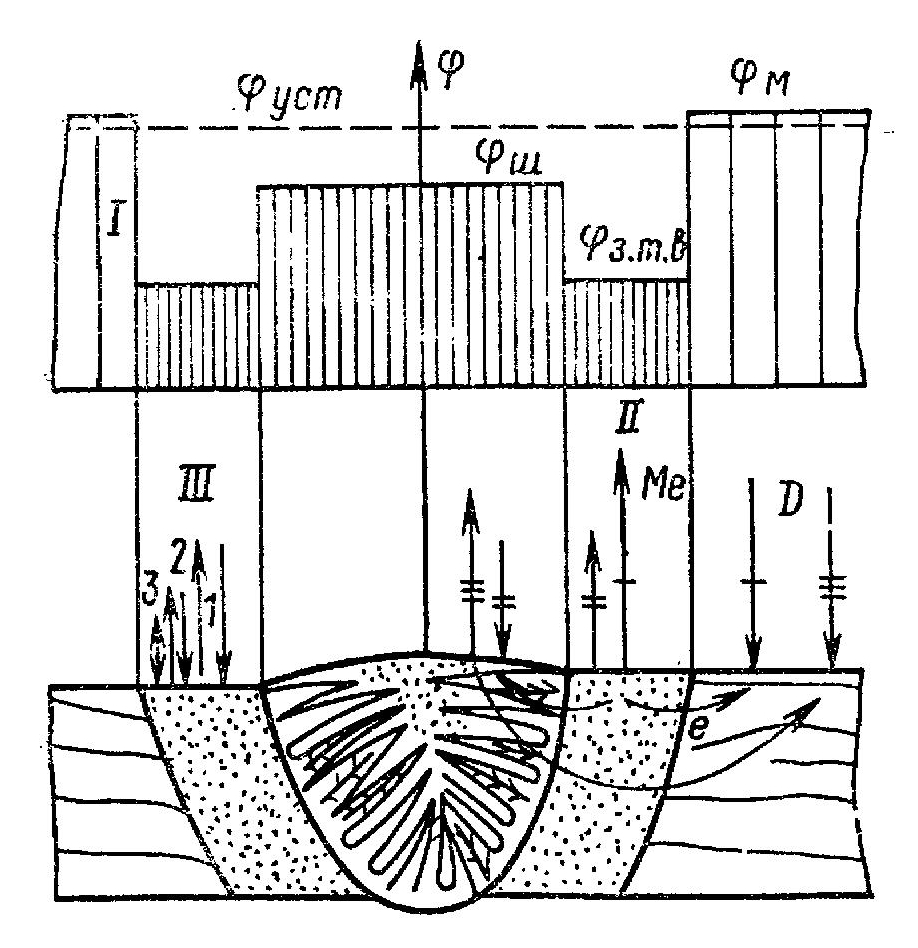
Рис. 3. Схемы коррозии сварного соединения: I – характерное распределение начальных макропотенциалов в сварном соединении; φш – электродный потенциал шва; φзтв – электродный потенциал зоны термического влияния; φм – электродный потенциал основного металла; φуст – установившийся стационарный потенциал заполяризованной системы шов – зона термического влияния (з.т.в.) – основной металл; II – макроэлектрохимическая коррозия, макропара основной металл– зона термического влияния, макропара зона термического влияния – шов, макро- пара основной металл – шов с зоной термического влияния; III – коррозия саморастворения каждой зоны: 1 – гетерогенный механизм электрохимической коррозии; 2 – гомогенный механизм электрохимической коррозии; 3 – химическая коррозия
Поэтому в коррозионном отношении сварное соединение представляет собой сложную многоэлектродную короткозамкнутую электрохимическую систему, характерными макроэлектродами которой являются шов, зона термического влияния с серией переходных структур, основной металл (табл. 1).
Таблица 1. Электродные потенциалы различных зон сварных соединений в З%-ном NaCl
|
Материал |
Способ сварки |
Электродный потенциал, мВ |
||
|
Основной металл |
Сварной шов |
Зона термического влияния |
||
|
Стали низкоуглеродистые низколегированные |
||||
|
09Г2С 17Г2С1 17Г2СФ |
Ручная дуговая, электрод типа Э55 |
-460 -500 -455 |
-540 -540 -540 |
-480 -550 -485 |
|
Коррозионностойкие стали |
||||
|
12Х18Н10Т 10Х14АГ15 |
Аргонодуговая Ручная без присадки, электролы ОЗЛ8 |
+137 -170 |
+108 -165 |
+75 -250 |
|
Алюминиевые сплавы |
||||
|
АМг6 АМг62 |
Аргонодуговая без при- садки |
-492 -680 |
-514 -700 |
-567 -880 |
|
Технический титан |
||||
|
ВТ1-1
Цирконий Тантал Ниобий |
Аргонодуговая без присадки
Электронно-лучевая |
-125
-455 -180 -241 |
-180
-393 -240 -255 |
-140
-446 -212 -280 |
Макронеоднородность оценивается по величине средних электродных потенциалов φ каждой зоны, микронеоднородность – по величине локальных электродных потенциалов φi в пределах каждой зоны. Показателем макроэлектрохимической неоднородности сварного соединения является разность начальных потенциалов Δφ между зонами. Показателем микронеоднородности каждой зоны служит разброс начальных локальных потенциалов Δφi = φi max – φi min в пределах каждой зоны.
Восприимчивость сварного соединения в целом или какой-либо его зоны к воздействию коррозионных сред и скорости коррозии зависит от общих и локальных электродных потенциалов и поляризуемости. Чем отрицательнее потенциалы и больше их разность, тем, как правило, больше скорость коррозии.
В зависимости от значений Δφ и Δφi возможны следующие характерные случаи общей коррозии сварных соединений:
- а) Δφ>0, Δφi→0, – коррозия по преимущественно макрогетерогенноэлектрохимическому механизму. Определение Δφ и Δφi позволяет в первом приближении судить о неустойчивости различных зон и всего соединения в целом;
- б) Δφ→0, Δφi>0 – коррозия по преимущественно микроэлектрохимическому механизму;
- в) Δφ>0, Δφi>0 – смешанный механизм коррозии.
Общая (сплошная) электрохимическая коррозия характерна для сварных конструкций из углеродистых и низколегированных сталей в большинстве природных сред (атмосфере, водных средах, почве).
Местные избирательные виды коррозии характерны для сварных соединений высоколегированных сталей и цветных металлов в средах, в которых металл находится в пассивной и пассивно-активной области. Межкристаллитная коррозия, связанная со структурными изменениями в сталях, характерна при воздействии на них нагрева до критических температур 450 – 900°С для аустенитных и выше 900°С для высокохромистых ферритных сталей. Примером является межкристаллитная коррозия сварных соединений аустенитных хромоникелевых сталей. Разрушение развивается в трех зонах:
- в основном металле, нагреваемом при сварке до 500 – 900°С,
- в сварном шве
- и в основном металле вблизи линии сплавления в узкой зоне, нагреваемой до температур свыше 1200 – 1250°С (ножевая коррозия).
Преимущественное разрушение границ зерен обусловлено электрохимической неоднородностью металла, возникающей при определенных для каждого сплава температурно-временных условиях в связи с выделением избыточных фаз. Если избыточные фазы образуют протяженные цепочки по границам зерен, то коррозионное разрушение приобретает чрезвычайно опасный межкристаллитный характер. Наиболее характерными избыточными фазами коррозионно-стойких сталей, практически постоянно в них присутствующими, являются карбиды. В зависимости от химического состава стали и условий термического воздействия на них образуются карбидные фазы следующих типов: МС (М≡ Тi, Nb, W, Zr, Ta); М2С (М≡ W, Мо); М3С (на основе железа); М7С3 и М23С6 (на основе хрома), М'nМ"mС (М'≡ Fe, Ni, Со, Si, M"≡ W, Мо, Та, V, Cr, Nb); часто n+m = 6; М12С. Наряду с карбидными возможно образование других фаз, представляющих собой соединения компонентов стали с неметаллами (нитриды, карбонитриды, сульфиды, бориды и др.), а также интерметаллидных фаз (σ, χ), ряд фаз типа Лавеса (Fe2Мо, Fe2W, Fe2Nb), упрочняющих фаз (M3Ti, М3Al) и др.
Принципиальная схема влияния температурно-временных условий на выделение карбидов и межкристаллитную коррозию показана на рис. 4. Температуры ≤850°С благоприятны для преимущественного выделения M23C6 (кривая 1). Ножевая коррозия связана с выделением цепочки карбидов стабилизирующих элементов (МС) под действием высоких температур (> 1200 – 1250°С) по границам зерен (околошовной зоны). Так как скорость коррозии (кипящая 56% HNO3) карбида титана примерно в 1000 раз, а карбида ниобия в 3 – 4 раза больше, чем скорость коррозии стали, то происходит избирательное растворение частиц карбидов, расположенных по границам зерен при катализирующем действии этого процесса на растворение прилегающих участков стали. Дополнительное тепловое воздействие в области критических температур (наложение второго шва) приводит к выделению карбидов хрома (M23C6), что усложняет механизм ножевой коррозии и повышает ее скорость. В окислительных средах кислотостойкие хромоникелевые стали, стабилизированные титаном, менее стойки, чем стабилизированные ниобием, которые, в свою очередь, менее стойки, чем с низким содержанием углерода.
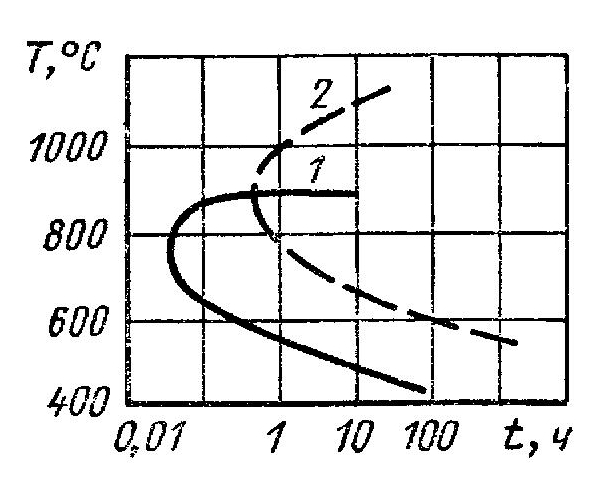
Рис. 4. Границы выделения карбидов типа M23C6(1) и МС (2) у сталей типа 12Х18Н10Т, нагретых до 1250°С, в зависимости от температурно-временных условий
Межкристаллитная коррозия алюминиевых сплавов также связана с выпадением избыточных (интерметаллидных) фаз типа CuAl2, Mg2Al3, MgZn2 и др.
Точечная коррозия типична для пассивирующихся металлов (хром, алюминий, хромо-никелевые стали и др.) и возникает в результате повреждения в отдельных участках пассивной пленки. В сварных соединениях точечной коррозии подвержена преимущественно зона термического влияния.
Коррозионное разрушение сварных соединений в напряженном состоянии.
Напряженное состояние влияет на коррозионное поведение металла вследствие:
- а) сообщения металлу добавочной энергии, в связи с чем иону Me+ легче покинуть решетку деформированного металла по сравнению с недеформированным;
- б) нарушения под действием деформации сплошности и защитных свойств поверхностных пленок;
- в) повышения степени неоднородности, связанной с появлением под действием деформаций дефектов кристаллической решетки и новых анодных фаз.
Скорость коррозии q относительно мало изменяется под влиянием упругих напряжений в нейтральных и щелочных средах, но может заметно (в 2 – 3 раза) увеличиваться в кислых средах пропорционально напряжениям: q=q0+ασ, где q0 – скорость без растягивающих напряжений; α – коэффициент пропорциональности. Незначительно влияя на общую коррозию, напряжения интенсифицируют местные виды коррозии, наиболее опасными из которых является растрескивание, вызываемое статическими нагрузками, и коррозионная усталость при циклическом нагружении.
Коррозионное разрушение в напряженном состоянии определяется коррозионными, механическими и сорбционными процессами, а также сопутствующими процессами (кавитация, радиация). Коррозионное растрескивание состоит из двух основных периодов:
- а) зарождения трещины или инкубационного периода (tэ), в течение которого на металлической поверхности под влиянием локализации коррозионного процесса и растягивающих напряжений происходит зарождение первичных коррозионно-механических трещин;
- б) периода развития трещины (tр), который, в свою очередь, определяется временем докритического (субкритического) роста трещины до ее критических размеров, после чего происходит лавинообразное разрушение.
Скорость субкритического роста коррозионных трещин в зависимости от материала, напряжений и среды изменяется в пределах .10 – 1О-5мм/ч.
Постоянное разрушение пленки и интенсивное перемещение раствора при циклическом нагружении может резко повысить скорость разрушения при коррозионной усталости по сравнению с коррозионным растрескиванием.
Разрушения вызываются растягивающими напряжениями. Для большинства сочетаний металл – среда имеются пороговые значения напряжений σпор, ниже которых растрескивание не имеет места вообще или на определенной базе испытаний (рис. 5). Пороговые напряжения варьируются в пределах (0,2 – 1) σт (табл. 2). Сварные соединения растрескиваются интенсивнее по сравнению с основным металлом в связи с воздействием сварочного процесса. Остаточные сварочные напряжения без внешней нагрузки могут вызывать интенсивное растрескивание (рис. 5, б). В средах, вызывающих растрескивание, действие остаточных напряжений и напряжений от внешней нагрузки суммируется (рис. 5, в).
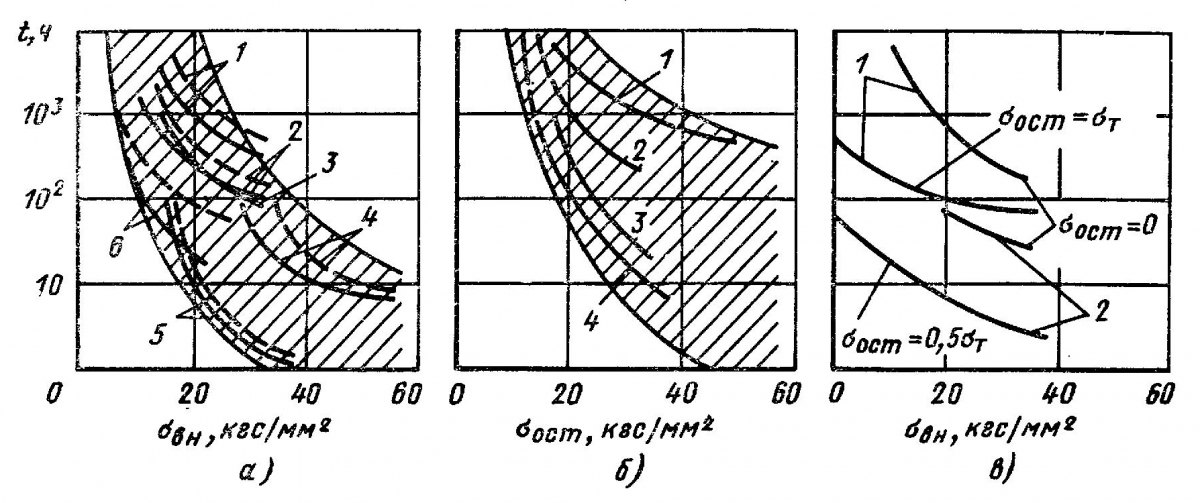
Рис. 5. Влияние напряжений и вида напряженного состояния на коррозионное растрескивание в различных средах (сплошные линии – сварное соединение, штриховые – основной металл):
а – σвн > 0, σост= 0; 1, 4 – одноосный изгиб; 2 – двухосный изгиб, 3, 5 , 6 – одноосное растяжение; 1, 2, 3 – 12Х18Н10Т; 4 – ОТ4; 5 – СтЗсп; 6 – АМг6;
б – σвн= 0, σост > 0; 1 – 12Х18Н10Т; 2 – ВТ1-1; 3 – СтЗсп; 4 – ОТ4; в – σвн> 0, σост> 0 – 12Х18Н10Т; 2 – ОТ4; среды – см. табл. 3
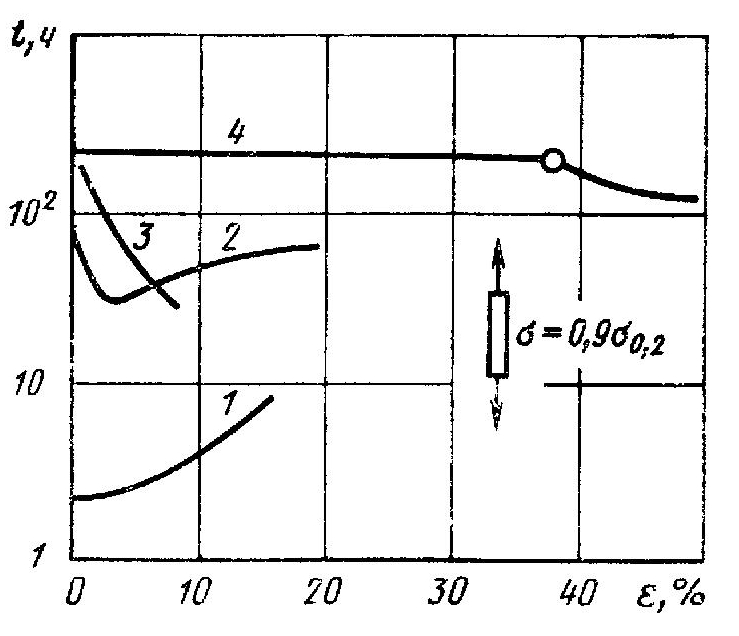
Рис. 6. Влияние предварительной пластической деформации растяжением на время до коррозионного растрескивания стали СтЗсп (1), 12Х18Н10Т (2), сплава АМг6 (3) и деформации сжатием сплава АМг6 (4). Коррозионные испытания при постоянной нагрузке σ= 0,9σт
Влияние пластической деформации на коррозионное разрушение не однозначно (рис. 6), так как в результате пластической деформации могут возникать как благоприятные, так и неблагоприятные изменения свойств металла и напряженного состояния. К неблагоприятным относятся:
- а) повышение внутренней энергии металла;
- б) возникновение при деформации анодных фаз, дефектов решетки, микро- и макронарушений поверхности и структуры, сопровождающихся увеличением и концентрацией напряженности II рода;
- в) возникновение при неравномерной пластической деформации собственных растягивающих напряжений I рода.
Процессами, способствующими повышению стойкости, являются:
- а) уменьшение, перераспределение и снятие в процессе деформации собственных напряжений I рода, а также возникновение сжимающих напряжений на поверхности;
- б) более равномерное распределение анодных участков, что уменьшает локализацию коррозионного разрушения.
В зависимости от металла и среды, деформационно-силовой схемы, степени деформации и термодеформационных условий превалируют те или иные процессы и имеет место увеличение или уменьшение стойкости металла. Отрицательное влияние концентраторов особенно резко- проявляется в средах, в которых металл находится в пассивном или активно-пассивном состоянии. С увеличением агрессивности сред влияние концентратора ослабевает. Чем выше уровень напряженности, тем сильнее проявляется влияние концентраторов при относительно меньшем влиянии среды,
Таблица 2. Ориентировочные значения отношения пороговых напряжений к пределу текучести некоторых материалов в характерных средах, вызывающих их растрескивание
|
Материал |
Среда |
Температура, °С |
Основной металл |
Сварные соединения |
|
Углеродистые и низколегированные стали |
Щелочные растворы Растворы нитратов Среды с сероводородом |
Т>60°С Кипение Нормальная |
0,9-1 0,5 0,5-1 |
0,9-1 0,5 0,3-0,5 |
|
Коррозионно-стойкие хромоникелевые стали типа 12Х18Н10Т: отожженные деформированные |
Хлориды |
Кипение |
0,5-0,6 0,2-0,5 |
0,4-0,5 0,2-0,4 |
|
Алюминиевые сплавы |
Растворы на основе З%-ного NaCl |
Нормальная |
0,6 |
0,5 |
|
Титановые а-сплавы |
Бромисто-метаноловые |
Нормальная |
0,5 |
0,2-0,4 |
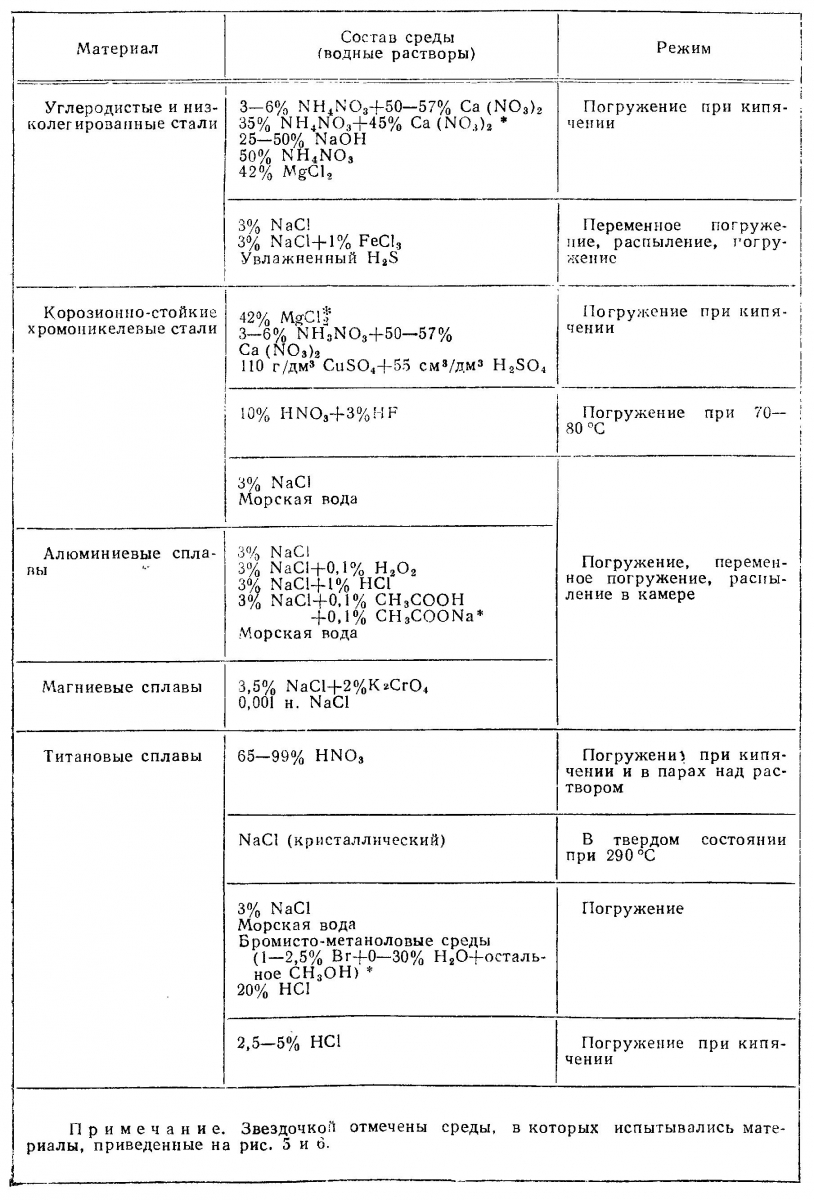
Таблица 3. Составы сред, рекомендуемых для ускоренных испытаний сварных соединений на склонность к коррозионному растрескиванию
- Войдите, чтобы оставлять комментарии
